Előállítása argon és hélium
A hélium és annak előkészítése
Tulajdonságok hélium. Hélium fedezték fel 1868 a nap megfigyelésével napfogyatkozás. 1895-ben találtak rá a földön.
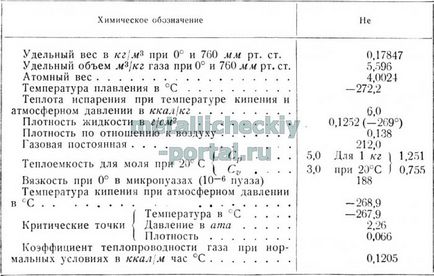
Hélium (He) teljesen inert gáz színtelen és szagtalan. Néhány fizikai állandóit a táblázatban mutatjuk be a hélium. 9. Nem szorbeálódik a szilárd és olvadt fémek.
9. táblázat Néhány fizikai állandók a hélium
Használata hélium. Úgy véli, a legnagyobb alkalmazás űrrepülés hélium töltés és a különböző léghajók légi járművekben.
Hélium nem éghető és robbanásveszélyes. Annak ellenére, hogy ő majdnem 2-szer nehezebb, mint a hidrogén, emelje kevesebb, mint a hidrogén csak 8%.
A hélium nagy használatra, mint a helyettesítő a nitrogén hígításban felhasznált oxigén a légzéshez. Előállítása 20% oxigén és 80% héliumot a kémiai tulajdonságai eltérnek a levegő, de mielőtt ez több előnnyel jár.
Hélium alkalmazunk finomítóanyag során olvasztására és öntésére színesfémek, különösen az alumínium és ötvözetei. Öblítôfurat folyékony fém jet eltávolítja hélium oldott gázok a fém, és távolítsa el a salak, mint a nem-fémes szennyeződéseket A12O3. Védő álló közegben hélium az öntés magnézium ötvözetek nullára csökken a hulladék, a szokásos öntési levegőn. Égésgátló és egy nagy hővezető hélium hagytuk alkalmazni, mint egy kioltó és a láng védőanyagként a tároló gyúlékony anyagok (benzin, gázolaj, stb).
Hélium feltöltésére használt izzólámpák wolfram szálak.
Széles körű használata hélium és más közömbös gázok a saját elektromos miatt a következő előnyökkel rendelkeznek összehasonlítva más gázok (hidrogén, nitrogén, stb ...):
1) kis ellenállású áthaladását a töltött részecskék;
2) alacsony önkisülés gyújtás potenciál;
3) a kis értékei gradiens a pozitív oszlop, attól függően, hogy a nyomás és a jelenlegi;
4) nagy elektron mobilitást annak a ténynek köszönhető, hogy a kevésbé kritikus potenciál fordul elő csak rugalmas ütközések elektronokkal energia.
Az elmúlt években, a hélium került sor ívhegesztő célokra védőgáz. A teljes hélium tehetetlenségi ez megakadályozza, hogy a megolvadt fém reakcióba a levegővel. Amellett, hogy befolyásolja a hegesztés kohászat, hélium, amint a fentiekből kitűnik, az ív stabilizálódik és generálja a különleges feltételeket a hő hatására a fém ív hegesztési.
Forrásai hélium. Hélium a termék a radioaktív bomlás. Ez tartalmazza az ásványi anyagok, amelyek egyszerre tartalmaznak urán vagy tórium.
radioaktív bomlás gázok miatt széles körű elterjedése a radioaktív anyagok keletkeznek mindenütt. Hélium képződik lassú, de folyamatos, de mivel a hatalmas tömegek a rock képződött hatalmas mennyiségű hélium - mintegy 25 millió köbméter 3 év ..
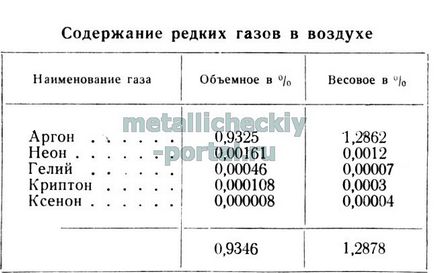
Hélium megtalálható kőzetek, az enyém gázok, gázok ásványvízforrás és vulkánok. Van egy nagy mennyiségű hélium a földgáz, amelynek egy része a metán és etán. Ezen túlmenően, ezek a földgáz tartalmaz nagy mennyiségű szén-dioxid és a nitrogén, valamint egy kisebb szennyeződést argon és egyéb nemesgázok.
Első hélium. Hélium nyerik földgázból (frakcionált kondenzációval, amely a következő: a természetes gázt összenyomják, és lehűtik, ahol a szennyeződések, amelyek magasabbak, mint a hélium, kondenzációs hőmérséklet, cseppfolyóssá hélium, amelynek nagyon alacsony a cseppfolyósítás hőmérsékletét (-269 ° C-on ) marad gáz halmazállapotú, és a bemutatott formában.
Ipari üzemek termelő hélium, részletesen az irodalomban.
A kis mennyiségű hélium lehet beszerezni, mint melléktermék a berendezés szétválasztás oxigén és nitrogén a levegő. Ezzel szemben a argon, hélium kiválasztása a levegő szétválasztó berendezés nem sok nehézséget.
Argon és fogadása
Argon tulajdonságai. Argon (Ar vagy A), valamint a hélium, egy egyatomos inert gáz.
Néhány fizikai tulajdonságai táblázatban vannak felsorolva argon. 11.

Az argon. Argon általánosan használt töltésére izzólámpák, hogy csökkentse a párolgási sebesség az izzószál és növeli a lámpa élettartama.
Ahelyett, hogy a tiszta argont használunk argon-nitrogén-elegyben (úgynevezett technikai argon, a tisztítás oxigén és nedvesség), ami legfeljebb 18% nitrogént; Ez azért van, mert a tiszta argont potenciálja alacsony öngyulladáshoz a kisülési, amelyek szikrázást a lámpában. nitrogénszennyeződés növeli a lehetséges gyulladási.
Argon egy nagyon széles körben használt elektromos vákuum technológiát.
Argon, valamint a hélium, használunk finomítás fémek öntése. Például argon használható finomításra rozsdamentes acél öntés során. A szerepe az inert gáz finomítás során az, hogy eltávolítjuk a hidrogén oldott folyékony fém. Az inert gáz, tehát pusztán fizikai beavatkozás. Az olvadt fémet átfúvatjuk inert gázzal. Mivel a hidrogén-az olvadt fém egy bizonyos nyomást, hogy kidiffundál a fém, közömbös gázbuborékok és felvitte a légkörbe.
Az inert gáz nem oldódik az olvadt fém és a „mosás” őket, hogy az olvadt fém az nem hat hátrányosan rajta.
1942-ben, ez készít egy új módszer a magnézium előállításában a dolomit ferroszilíciumot és argon, mint az inert közegben. Széles körű használata tiszta argon a termelés fénycsövek (CFL-ek), amelyek többször gazdaságosabb, mint az izzók.
A közelmúltban, valamint hélium, argon alkalmazunk, védő inert atmoszférában során ívhegesztő számos fémek és ötvözetek. Így minden esetben egy tisztaságú argon különleges követelmények. Ezek a követelmények függvényében változtathatók a hegesztési körülmények márka hegeszthető anyagból, elektróda anyaga, és így tovább. N. konkrét utalásokat adnak erről a vonatkozó fejezetekben a könyv.
Előállítása argon. Argon iparilag előállított, mint melléktermék előállítására oxigén és nitrogén a levegőből. A folyamatot megszerzésének argon áll a következő lépéseket: a) cseppfolyósítását környezeti levegő; b) desztillációs folyékony levegőt annak érdekében, hogy elválassza azt alkotórészeire és a termelő argon-nitrogén-oxigén keverék (ún nyers argon); c) tisztítási nyers argon.
Cseppfolyós levegő desztilláljuk. Mivel argon forráspontja feletti forráspont nitrogén 10 °, és forráspontja alatti oxigén 3 °, majd torlódás fordul elő argon az oxigén-nitrogén keverék elhagyja a meghatározott részét a desztillációs oszlop.
A további desztillációs az elegy elérte a több magas tartalma argon. További tisztítását Ezt a keveréket (a nyers argon) van előállítva oxigén vegyi úton, égetéssel ott kén- vagy hidrogénatom. Ennek eredménye egy gázt tartalmazó argon, vízgőz, nitrogén és némi oxigént. Ez a gáz elegyet vezetjük át forró réz-oxid és a tiszta réz. A hidrogént birtokában helyreállítása és réz-oxidot képezve vízgőz, és réz oxigénnel kombinálódik. Nyert ezen gáz (az úgynevezett technikai argon) tartalmazó 82% vagy több, argon, összenyomódik, és a fogyasztónak szállított.
Műszaki argont is tisztíthatjuk, mélyhűtés és frakcionált desztillációval. Ily módon szinte az összes nitrogén eltávolítása. Maradékait akkor eltávolítható argon átvezetésével át forró kalcium.
Az új előírások Glavkislorod tiszta argont desztillációjával kapott technikai argon. Tiszta argont lemerült két kompozíció: № № 1 és 2 tiszta argont készítmény Ar № 1 tartalmaz (térfogat% -ban)> 99,7 és szennyeződések (térfogat%): nitrogén <0,24%, кислорода <0,05% и двуокиси углерода <0,01%. Чистый аргон состава № 2 содержит аргона> 99,2%, és a szennyeződések: nitrogén <0,55%, кислорода <0,2% и двуокиси углерода <0,05%. Капельная влага отсутствует.